研究紹介
川村研究室では固体NMR分光法を用いて、生体分子が機能する上で必要な立体構造や運動性を明らかにし、生体分子の働きを分子レベルで理解すること(構造-機能相関)を目指しています。また、新規分子設計・合成・構造物性解析を通して天然にはみられない新しい機能や性能を向上させる研究を行い、機能性生体材料の開発を目指しています。
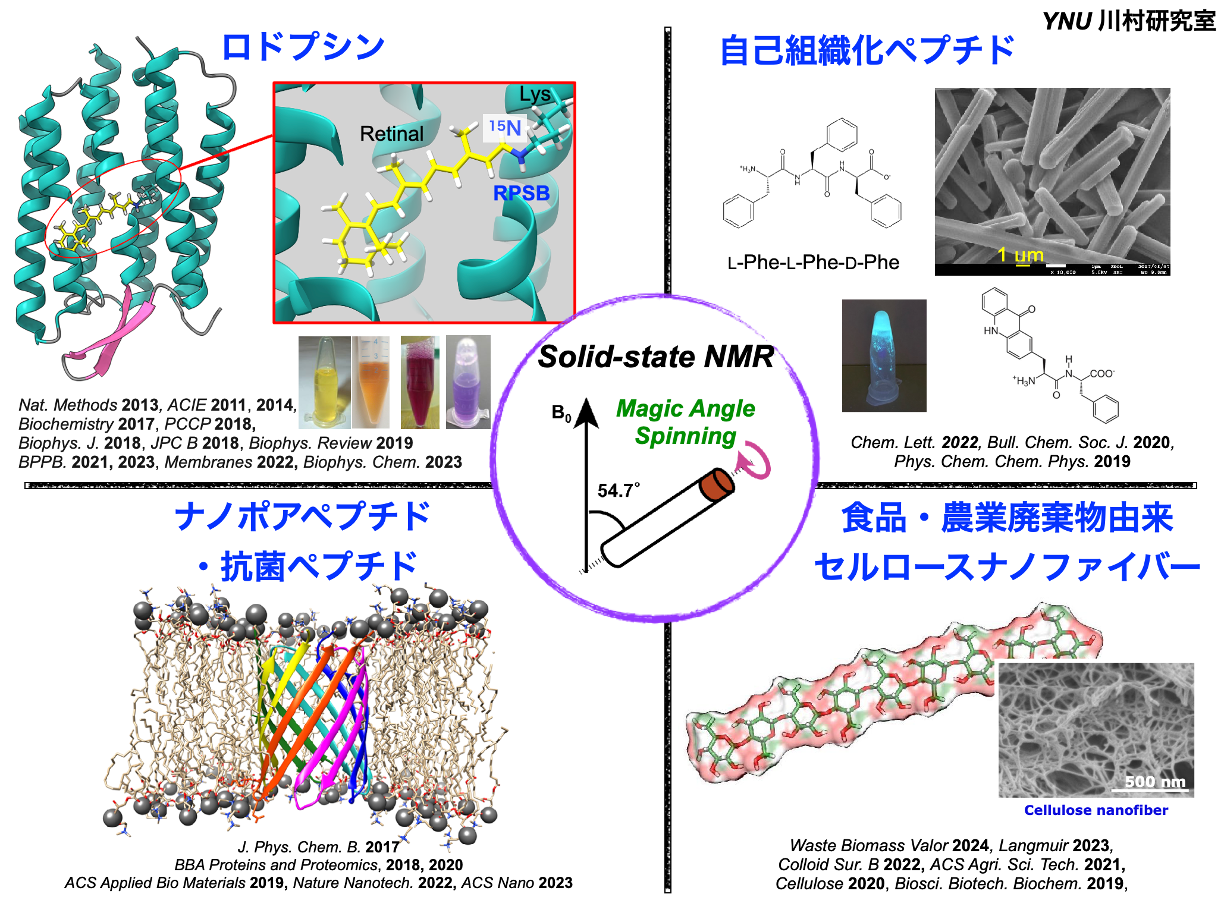
最近の研究トピックスは 微生物型ロドプシン(Microbial rhodopsin)、抗菌性ペプチド(Antimicrobial peptides)、自己組織化ペプチド (Self-assembly)、セルロースナノファイバー (cellulose nanofiber) です。
●微生物型ロドプシン
生体分子の中でも細胞膜上の膜タンパク質は信号伝達、イオン透過、物質輸送などを制御して生命活動に重要な役割を果たしています。7回膜貫通型のロドプシンタンパク質はレチナールとその周辺アミノ酸残基との相互作用により、機能と色が制御されており、オプトジェネティクスの基盤的な役割を果たしている。固体高分解能NMRによってレチナールおよびその周辺アミノ酸残基との相互作用を調査し、機能発現メカニズムを明らかにするための研究を行っている。
●抗菌ペプチド・ナノポアペプチド
細胞膜は抗菌活性ペプチドの反応場として注目を集めている。また、1分子センシングが可能とされているナノポアペプチドも細胞膜で働いている。このような細胞膜に結合した状態の分子構造情報を得ることは難しい課題であるが、固体高分解能NMRの手法をはじめとした物理化学計測を駆使して、細胞膜結合分子との構造と機能の相関を分子論的に明らかにする研究を行っている。
●自己組織化ペプチド
水中などでペプチド同士を会合させ、超分子形成するペプチドの分子設計および超分子構造を調べ、新規生体材料開発の研究を行っている。
●食品・農業廃棄物由来セルロースナノファイバー
コーヒー粕やホップつる由来のセルロースナノファイバーの単離およびその応用研究を行っている。